2025年度(令和7年度)日本内分泌学会研究奨励賞は 5名の先生方が受賞されました。
これまでのキャリアや若手の先生方へのメッセージをご寄稿下さいましたのでご紹介いたします。
皆様のロールモデルとしてぜひご参考になさってください!
 |
馬越 洋宜 (九州大学大学院医学研究院 病態制御内科学) 副腎皮質腫瘍の分子病態の解明と診断法の確立 |
 |
佐久間 一基 (千葉大学大学院医学研究院 分子病態解析学) 先天性酵素欠損症における肝糖脂質代謝の病態生理の解明 |
 |
|
 |
|
 |
馬越 洋宜(九州大学大学院医学研究院 病態制御内科学)
受賞タイトル:
副腎皮質腫瘍の分子病態の解明と診断法の確立
 このたびは、日本内分泌学会研究奨励賞という名誉ある賞を賜り、心より光栄に存じます。これまでご指導くださった小川佳宏先生をはじめ、多くの先生方、そして日々ともに研究に励んでいる研究室の皆様に、深く御礼申し上げます。
このたびは、日本内分泌学会研究奨励賞という名誉ある賞を賜り、心より光栄に存じます。これまでご指導くださった小川佳宏先生をはじめ、多くの先生方、そして日々ともに研究に励んでいる研究室の皆様に、深く御礼申し上げます。
私は臨床医の立場から研究に取り組んでまいりましたが、今回の受賞に至るまでの経緯について、3つの観点から共有させていただきます。若手の先生方にとって、少しでも参考や励みになれば幸いです。
第一に、研究の原点は臨床における素朴な疑問でした。研修期間中、市中病院にて多数の原発性アルドステロン症(PA)症例に触れる機会を得ましたが、当時は診療方針を裏付けるエビデンスが限られており、日々の診療で生じるクリニカル・クエスチョンが研究を志すきっかけとなりました。この疑問を解決すべく、PAの多施設共同研究を主導されていた国立病院機構京都医療センターの成瀬光栄先生のもとで学び、現在の診療ガイドラインにも反映される成果を得ることができました。研究キャリアの出発点として、豊富な臨床データと優れた指導環境の下で取り組めたことは、私にとって大きな財産となりました。臨床医が研究に取り組む際には、現場での気づきを起点としながら、柔軟に最適な環境を選ぶ姿勢が非常に重要であると感じています。
第二に、病態解明に向けたアプローチの転換です。臨床研究を通じて、PAという1つの疾患の中にも多様な表現型が存在することを実感し、分子基盤から病態を理解する必要性を強く感じるようになりました。そこで、分子生物学的手法を用いた病態解明を目指し、現在所属する九州大学の小川佳宏先生のもとで疾患基礎研究に取り組む機会を得ました。しかし当初は、オリジナリティのある研究テーマを構築することに苦慮し、方向性が定まるまで1~2年を要しました。そのような中、小川先生より以前からテーマとして提案されていたものの、実験の難しさから進展していなかったシングルセル解析について、埼玉医科大学国際医療センター・西本紘嗣郎先生がヒト副腎サンプルでのデータ取得に成功され、私はその解析担当として参画することができました。
シングルセル解析は、1検体からでも高精度な病態情報を得られる手法であり、リソースの制約がある中でも成果に結びつきやすく、私にとって大きな転機となりました。技術導入から安定した成果を得るまでに約5年を要しましたが、その過程で研究の中長期的な進捗を支えていただける環境の重要性を改めて実感しました。また、研究が高度化するにつれ、個人の努力だけでは解決が難しい局面も多くなり、的確な視点で助言をくださる小川先生や、データをもとに忌憚のない議論ができる研究室のメンバーなど、環境を構成する「人」の力の大切さも日々痛感しています。技術の進歩により、ヒト検体を用いた分子病態解析も現実的となり、臨床と基礎の距離は確実に縮まってきていると感じています。
第三に、「継続することの大切さ」を学びました。一つのテーマに10年以上取り組むという経験は初めてでしたが、時間をかけてこそ得られる視点があることを実感しました。臨床と基礎の双方の視点を持つことで、エビデンスが乏しい領域でも、より多角的に物事を判断・解釈できる力が養われたと感じています。また、研究活動を通じて得られた多様な人的交流や視座は、仕事のみならずプライベートの場面でも大きな財産となっています。
若手の先生方にお伝えしたいのは、研究は臨床から離れたものではなく、むしろ密接に結びついているということです。一見遠回りに思える過程も、そこから得られる副次的な学びや出会いは非常に大きく、もし少しでも興味を持つテーマがあるのであれば、ぜひ適切な環境で取り組んでみてほしいと思います。
最後になりましたが、本賞の受賞は、これまでご指導くださった先生方、共同研究者の皆様、そして日々の診療を通じて学びの機会を与えてくださった患者の皆様のおかげです。心より感謝申し上げますとともに、今後も内分泌学の発展に微力ながら貢献してまいります。
略歴
2009年3月 熊本大学医学部医学科 卒業
2009年4月 熊本大学医学部附属病院 初期研修医
2010年4月 国保水俣市立総合医療センター 初期研修医
2011年4月 松山赤十字病院 内科 後期研修医
2014年4月 国立病院機構京都医療センター 臨床研究センター 内分泌代謝高血圧研究部 研究員
2015年4月 国立病院機構京都医療センター 内分泌代謝内科 レジデント
2016年4月 国立病院機構京都医療センター 内分泌代謝内科 医師
2019年4月 九州大学病院 内分泌代謝・糖尿病内科 特任助教
2023年8月 九州大学大学院医学研究院 病態制御内科学 助教
佐久間 一基(千葉大学大学院医学研究院 分子病態解析学)
受賞タイトル:
先天性酵素欠損症における肝糖脂質代謝の病態生理の解明
 このたびは栄誉ある日本内分泌学会研究奨励賞に選出いただき、大変光栄に存じます。千葉大学の田中知明先生・横手幸太郎先生をはじめ、これまでご指導いただいた先生方、サポートいただいた同僚の皆様に感謝申し上げます。
このたびは栄誉ある日本内分泌学会研究奨励賞に選出いただき、大変光栄に存じます。千葉大学の田中知明先生・横手幸太郎先生をはじめ、これまでご指導いただいた先生方、サポートいただいた同僚の皆様に感謝申し上げます。
学生時代、ホルモン分泌制御を論理的に考えることができる点に魅力を感じ、内分泌学に興味を抱きました。新潟大学卒業後は新潟市民病院で初期研修および救急科後期研修を行い、救急科の廣瀬保夫先生から「臨床現場で遭遇する印象的な症例は論文化すること」を教えられました。救急科での後期研修は1年間と短い期間でしたが、廣瀬先生のご指導の下、溺水を契機とした EBV 関連血球貪食症候群、電撃性紫斑病を伴う劇症型肺炎球菌感染症、肝損傷に伴う胆汁性腹膜炎、メタノール中毒の血中代謝産物測定など、救急外来・集中治療室で経験した症例を考察し報告したこと(救急医学 2009, 2010;中毒研究 2010)は、「臨床の問いを研究へ」という現在の姿勢の礎となりました。
学生時代から抱いていた内分泌学への関心をさらに深めるため、千葉大学大学院医学研究院 内分泌代謝・血液・老年内科学(横手幸太郎教授)へ入局しました。横浜労災病院では西川哲男先生のご指導の下、副腎腫瘍におけるステロイド合成酵素の遺伝子発現解析を行い、アルドステロン産生腺腫の特徴を報告しました(Endocr J 2013)。続いて、田中知明先生・横手幸太郎先生のご指導を受け、異所性ACTH産生褐色細胞腫の症例を解析し、腫瘍が異なる2つの細胞系譜を有し、POMCのプロモーター領域の脱メチル化が異所性ACTH産生に関与していることを報告しました(J Clin Endocrinol Metab 2016)。さらに、リンパ腫様肉芽腫症が副腎不全を来す新たな病態を報告しました(Lancet 2024)。これらの経験から、既存の医学知識では説明しきれない現象に出会った際、分子生物学的手法でその背景のメカニズムに迫る醍醐味を感じるようになりました。
低血糖乳酸アシドーシスを呈した症例において、糖新生系酵素Fructose-1,6-bisphosphataseの新規変異をエクソーム解析から同定し、LC-MS/MS解析によるインタラクトーム解析と過去に報告された全てのミスセンス変異の機能解析を通じて、変異酵素のフォールディング異常が重要なことを報告しました(Commun Biol 2023)。本報告の機能解析を通じて、肝臓の糖代謝、脂質代謝機構に興味を持ち、代謝機能障害関連脂肪肝炎の病態解明に主眼をおいた研究を行いたいと考えるようになり、大きな転機となりました。
科研費「国際共同研究加速基金(A)」の支援を受け、肝臓糖脂質代謝研究の権威である Yale 大学 Gerald Shulman 教授との国際共同研究の機会を得ました。リゾホスファチジン酸や脂肪滴コレステロールが代謝機能障害関連脂肪肝炎の進展を促進し、GPAM と COASYの阻害が保護的に働くことを報告しました(PNAS 2023, 2025)。Shulman先生のPhysician scientistとして、基礎研究を臨床にどう結びつけるかを常に考える姿勢は大変参考になりました。また、Shulman研究室の多国籍の同僚と交流する中で、外国からみた日本の気づきがあったことや、彼らの研究に協力する機会もあり、貴重な経験を積むことができました。
内分泌学を志す若手の皆様には、「臨床現場で生じた問い」を探究する醍醐味をぜひ味わっていただきたいと思います。私自身は、希少内分泌代謝疾患(FBPase欠損症・異所性 ACTH 産生症候群)の病態解明を深めるとともに、脂肪毒性をターゲットとしたN-アセチルガラクトサミン修飾アンチセンスオリゴヌクレオチドを用いた代謝機能障害関連脂肪肝炎治療薬の臨床応用にむけた基盤の構築を目指し、若手の皆様とともに内分泌学の発展に少しでも貢献していきたいと考えています。
略歴
2006年 新潟大学医学部卒業、新潟市民病院初期研修医
2008年 新潟市民病院救急科シニアレジデント
2009年 千葉大学医学部附属病院糖尿病代謝内分泌内科シニアレジデント
2010年 横浜労災病院内分泌代謝内科シニアレジデント
2015年 千葉大学大学院医学薬学府博士課程修了、君津中央病院内分泌代謝科医長
2016年 千葉大学医学部附属病院臨床試験部特任助教
2019年 Yale大学Gerald Shulman研究室博士研究員
2020年 千葉大学大学院医学研究院分子病態解析学特任准教授
主な受賞歴
2011年 日本内分泌学会臨床内分泌代謝Update優秀演題賞
2012年 米国内分泌学会Outstanding Abstract Award
2014年 国際内分泌学会・米国内分泌学会合同会議International Travel Fellowship Award
2015年 日本内分泌学会若手研究奨励賞
2016年 日本内分泌病理学会研究賞最優秀賞
2018年 日本内分泌学会臨床内分泌代謝Update優秀ポスター賞
2019年 米国内分泌学会Outstanding Abstract Award
2024年 米国内分泌学会Early Career Forum Travel Award
松本 隆作(京都大学 iPS 細胞研究所 未来生命科学開拓部門)
受賞タイトル:
ヒト iPS 細胞を用いた下垂体疾患・発生研究
 この度は、日本内分泌学会研究奨励賞という大変栄誉ある賞を頂戴し、誠にありがとうございます。これまでご指導頂きました髙橋 裕 先生(奈良県立医科大学)、青井 貴之 先生(神戸大学)、須賀 英隆 先生(名古屋大学)、山本 拓也 先生(京都大学)には、心より深く御礼申し上げます。先生方の研究における高い志と、常に新しい視点を示してくださるご指導があってこそ、今回の成果にたどり着けたものと実感しております。
この度は、日本内分泌学会研究奨励賞という大変栄誉ある賞を頂戴し、誠にありがとうございます。これまでご指導頂きました髙橋 裕 先生(奈良県立医科大学)、青井 貴之 先生(神戸大学)、須賀 英隆 先生(名古屋大学)、山本 拓也 先生(京都大学)には、心より深く御礼申し上げます。先生方の研究における高い志と、常に新しい視点を示してくださるご指導があってこそ、今回の成果にたどり着けたものと実感しております。
私が内分泌学の、とりわけ研究に携わりたいと考えるようになったのは学部学生時代の病院実習での髙橋 裕 先生の講義がきっかけでした。ややもすると手を抜いてしまいそうな、6人の小グループに対する講義でしたが、内分泌学の基礎的な考え方から、当時明らかになってきたオキシトシンの愛着に関する話題などを、大変熱心に、そしてエネルギッシュにお話頂いたことを今でもよく覚えています。髙橋先生の熱量が伝わってくるとともに、内分泌学のロジカルな考え方と研究でこれまでわからなかったことを自分で明らかにしていくことの面白さに惹かれ、内分泌学を志すようになりました。
今回の研究課題は、その髙橋先生のもとに大学院へ進学して以降十年来続けてきたヒトiPS細胞から下垂体オルガノイドを誘導する技術を基盤にしたものです。この技術を用いて、下垂体疾患の病態解析やヒト下垂体発生機構の理解を目指して研究に取り組んで参りました。
臨床に従事するなか、下垂体疾患には原因が十分にわかっていない疾患や診断法や治療法が確立していない疾患が多く存在することを実感していました。その理由のひとつとして、下垂体のよい研究モデルがないことが挙げられると思います。これまで研究に用いることのできるようなヒトの下垂体細胞株は確立しておらず、臨床的にも下垂体疾患の臨床検体が得られる機会も限られています。そこで着目した手法が、名古屋大学の須賀先生らの開発されたヒトiPS細胞などの多能性幹細胞から下垂体オルガノイドを誘導する技術です。胎生期に下垂体は口腔外胚葉上皮から発生しますが、その分化過程では隣接する視床下部からのシグナルが必要です。この分化誘導法では、ひとつのオルガノイド内にこれらの異なる組織を同時に誘導することで下垂体の胎生期の分化過程を試験管内で再現することができ、実際に生理的な機能を有するホルモン産生細胞を誘導することができます。この技術を用いて最初に取り組んだのが、先天性下垂体機能低下症の疾患モデルの作製です。先天性下垂体機能低下症は既知の原因遺伝子が同定される率も低く、特にヒトの疾患モデルは存在しなかったため、その発症機序の解析は困難でした。OTX2変異を有する先天性下垂体機能低下症の患者さんからiPS細胞を樹立し下垂体オルガノイドへ誘導してみると、ホルモン産生細胞への分化が障害されるという表現型を得ることができました。さらにこの分化過程を経時的に解析していくことで、口腔外胚葉から下垂体前駆細胞への分化が障害されていました。その機序として、視床下部に発現するOTX2がFGF8やFGF10といったFGFファミリーの発現を制御することで、視床下部-口腔外胚葉間の組織間作用を介して下垂体発生に寄与するという機序を明らかにすることができました。この研究をはじめとして、他の先天性下垂体機能低下症の解析や、後天性の疾患として下垂体腫瘍のモデル作製、正常な下垂体発生機構の解析などいろいろな課題に挑戦させて頂いて来ました。これらの研究は、症例のリクルート、iPS細胞の樹立・培養、下垂体オルガノイドの誘導、解析といったプロセスを要し、多くの先生方のご指導、サポートなしでは成し得なかったものと実感しております。
これまでの研究を振り返ってみると、失敗や苦労の連続であったと思います。ヒトiPS細胞は毎日の培地交換が必要な上に、下垂体のオルガノイドの誘導には3か月以上を要するので、大学院入学以降は盆も正月もなく、風邪をひいても肺炎になっても連日細胞培養を続けてきました。誘導自体がうまくいかなくなってしまったことやコンタミですべての細胞がダメになってしまったことも一度や二度では済みません。苦労に見合った対価や成果が得られているとは到底思えませんが、何か新しいことを見つけたときの感動は何物にも代えがたく、研究を辞めたいと思ったことは一度もありません。残念ながら、私には目の覚めるようなアイデアや画期的な発明をできるような才能やセンスは備わっていないと自覚しています。それでも愚直に取り組んできたことが、今回の受賞につながったと考えております。現在は、この下垂体オルガノイド技術にゲノム編集、シングルセルトランスクリプトミクスなどの次世代シークエンサー技術、AIといった技術を融合することで新しい下垂体研究を展開できるように研究に取り組んでいます。こうした研究が将来的に疾患の病態理解や新規治療法の開発につながることを信じ、引き続き精進していく所存です。この度の受賞を励みに、さらに研究を発展させ、多くの患者さんに還元できる成果を生み出せるよう努力してまいります。改めまして、本学会の先生方、共同研究者の皆様、研究を支えてくださった皆様に感謝申し上げます。今後とも変わらぬご指導・ご鞭撻のほど、よろしくお願い申し上げます。
略歴
2003年 京都大学 理学部理学科 中退
2009年 神戸大学 医学部医学科 卒業
2009年 神戸市立医療センター中央市民病院 初期研修医
2011年 倉敷中央病院 内分泌代謝科 シニアレジデント
2013年 神戸大学大学院 医学研究科 入学
2014年 名古屋大学大学院 医学系研究科 特別研究学生
2017年 神戸大学大学院 医学研究科 卒業
2017年 神戸大学大学院 医学研究科 iPS細胞応用医学 博士研究員
2019年 京都大学 iPS細胞研究所 未来生命科学開拓部門 研究員
2020年 日本学術振興会 特別研究員 (PD)
2024年 京都大学iPS細胞研究所 未来生命科学開拓部門 特定拠点助教
主な受賞歴
2014年 ENDO Travel Grant
2017年 日本内分泌学会 若手研究奨励賞
2017年 日本内分泌学会 臨床内分泌代謝Update 優秀ポスター賞
2022年 日本内分泌学会 研究助成制度 若手研究者による研究課題
村上 正憲(東京科学大学病院 糖尿病・内分泌・代謝内科)
受賞タイトル:
腫瘍間・内不均一性に着目した副腎腫瘍の病態解析

このたびは、日本内分泌学会研究奨励賞という栄誉ある賞を賜り、誠に光栄に存じます。これまでご指導・ご支援くださった東京医科歯科大学(現・東京科学大学)糖尿病・内分泌・代謝内科の諸先生方、とりわけ内分泌領域の研究を始めるにあたり多大なるご指導を賜った小川佳宏教授(現・九州大学)、吉本貴宣先生(現・都立広尾病院)、そしてドイツ留学から帰国後、研究をさらに発展させる機会を与えてくださった山田哲也教授に心より感謝申し上げます。また、国内外の共同研究者の皆様、研究と臨床を支えてくださった多くの関係者の皆様にも、深く御礼申し上げます。
私は医学部入学以来、医学研究への関心を持ち、設置後2年目のMD-PhDコースにて在学中に基礎研究の世界へと足を踏み入れました。当時ご指導いただいた中村正孝教授(当時・東京医科歯科大学 疾患遺伝子実験センター)には、珍しい存在として可愛がっていただき、研究生活の初歩を学ばせて頂いた後、医学部卒業、臨床研修へと進みました。研究者のバックグラウンドを持てたこともあり、生体の恒常性維持という論理構造と、それが破綻した際の疾患としての姿、さらにその背景にある遺伝子異常などの分子機構が結びついたときの理解の深まりに強く惹かれ、内分泌・代謝領域に進むことを決意しました。
小川教授・吉本先生のご指導のもと、副腎腫瘍の分子生物学的解析に携わり、メチローム解析などのオミクス手法を用いた研究を開始しました(Eur J Endocrinol, 2015, Endocr Relat Cancer, 2017)。アルドステロン産生腺腫(APA)をはじめとする副腎腫瘍は、腫瘍性病変でありながら高いホルモン合成能(≒高分化?)を保持しており、「腫瘍化≒低分化」という枠組みに収まらない点に強く興味を持ちました。
幸運にも、副腎腫瘍研究で世界をリードするドイツ・ミュンヘン大学のBeuschlein教授(現・チューリッヒ大学病院)、Reincke教授の研究室に留学する機会を得て、そこで副腎腫瘍のメタボローム解析に取り組みました(JCI Insight, 2019, Eur J Endocrinol, 2021, Clin Chem, 2023)。同研究室は欧州副腎腫瘍研究ネットワーク(ENS@T)の中心的役割を担っており、国際共同研究の体制構築や学術的リーダーシップを間近に学ぶことができました。APAを対象とした解析では、留学前から着目していた体細胞変異と分子・臨床表現型との関連(genotype-phenotype correlation)に焦点を当て、特にKCNJ5変異を有するAPAの特徴を明らかにすることができました。
この段階までは、いわば「症例間の不均一性」に注目した解析でした。一方で、APAは腫瘍内においてもアルドステロン合成酵素の発現が不均一であることが知られており、腫瘍内不均一性が予想されていました。帰国後、東京医科歯科大学(現・東京科学大学)に復帰した際、山田教授の指導の元シングルセル解析の研究体制が立ち上がっており、これを副腎腫瘍に応用する取り組みを開始させて頂きました。既報がないため試行錯誤の連続でしたが、凍結検体から核を抽出し、高感度cDNA増幅法(TAS-Seq)を活用することで、副腎由来の腫瘍細胞を解析する手法を確立しました。典型的なAPAの3症例を解析したところ、各症例で細胞構成が大きく異なることが分かり、腫瘍内における分化経路の多様性が浮かび上がりました(Hypertension, 2024)。この知見は、APA発症の分子機構解明に資するのみならず、今後の内科的治療戦略の基盤となることを期待しています。
また、ENS@Tでの経験を活かし、成瀬光栄先生(医仁会武田総合病院)にご指導頂きながら国際共同研究を行っております。最近では原発性アルドステロン症の重症度分類の提唱を行いました(Eur J Endocrinol, 2025)。国際共同研究で本邦主導の発信を行うことで、微力ながら本学会の国際性に貢献出来ればと思っております。
振り返ってみますと、私の研究生活は、常に優れた指導者や仲間との出会いに恵まれ、背中を押していただいたことで歩みを進めることができたと実感し、感謝しております。また、研究留学の経験を通しても改めて感じたことですが、臨床家としての問題意識を持ちつつ、研究という視点から問いを立てるphysician-scientistの存在は、国際的にもますます希少かつ貴重なものになっていると感じています。大学院進学者の減少が懸念される昨今ではありますが、臨床・研究いずれの現場においても、課題意識をもって貪欲に可能性を追求する姿勢が、より一層求められているように思います。ともに歩む若い世代の皆さんと、少しでも前向きなエネルギーを分かち合えるよう、私自身も臨床と研究のあいだを往還しつつ挑戦を続けていきたいと考えております。引き続き、皆様のご指導・ご鞭撻を賜りますよう、何卒よろしくお願い申し上げます。
略歴
2008 東京医科歯科大学大学院医歯学総合研究科修了(MD-PhDコースにて医学博士取得)
2010 東京医科歯科大学医学部医学科卒業
2010 東京医科歯科大学医学部附属病院・初期臨床研修医
2011 東京都立墨東病院・初期臨床研修医
2012 東京都保健医療公社豊島病院内分泌代謝内科・医員
2013 東京医科歯科大学医学部附属病院 糖尿病・内分泌・代謝内科・医員
(2014 メディカルフェロー、2015 特任助教)
2017 Medizinische Klinik and Poliklinik IV, Ludwig-Maximilians-Universität München, Munich, Germany・Post-doctoral fellow
2020 東京医科歯科大学医学部附属病院(現:東京科学大学病院)糖尿病・内分泌・代謝内科・助教
主な受賞歴
2015 第38回日本高血圧学会総会Young Investigator’s Award 優秀賞
2019 18th ENS@T Scientific Meeting, ENSAT Award for APA research
2020 第93回日本内分泌学会総会 若手研究奨励賞
2021 第23回田中道子記念研究奨励賞(東京医科歯科大学医科同窓会)
2023 22nd ENS@T Scientific Meeting, ENSAT Award for NAPACA research
山内 一郎(京都大学大学院医学研究科 糖尿病・内分泌・栄養内科学)
受賞タイトル:
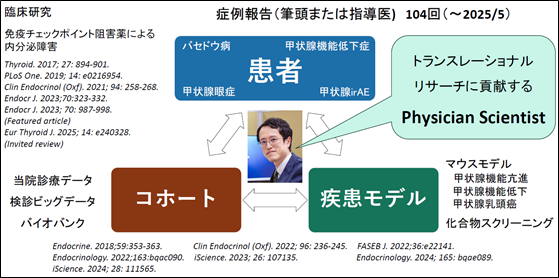
甲状腺ホルモン作用調節機構のトランスレーショナルリサーチ

このたびは、伝統ある研究奨励賞にご選出いただき、心より御礼申し上げます。歴代の受賞者の先生方のお名前を拝見し、身の引き締まる思いとともに、今後も内分泌学会に貢献できるよう精進してまいりたいと存じます。僭越ながらこれまでの経験を振り返りつつ、皆様に何らかのヒントとなればと思い、寄稿させていただきます。
私は、医学部卒業後の6年間、市中病院で臨床に専念しておりました。現在こそ大学で内分泌疾患の専門外来を担当しておりますが、当初は糖尿病など代謝疾患の診療が中心で、研究とも無縁の日々でした。研究者としてのスタートは決して早くありませんでしたが、今振り返ると、症例報告も含めた臨床経験が現在の研究活動の土台となっていると強く感じます。
大学院へ進学したのは、「皆が進む道だから」「研究にも興味があるから」といった、ごく一般的な動機でした。研究をライフワークにするという意識が最初からあったわけでもなく、「自分に合うかどうか、やってみないと分からない」という気持ちで飛び込みました。当時、甲状腺領域を専門とする教員がおられなかったのですが、稲垣暢也先生(現 田附興風会 医学研究所北野病院 理事長)が「やってみなさい」と背中を押してくださり、八十田明宏先生(現 京都医療センター 臨床研究センター長)には、専門分野を越えて研究の考え方や姿勢をご指導いただきました。私自身も、後進を指導する立場となった今、好奇心を刺激するようなテーマを一緒に考えることを大切にしています。
甲状腺研究の第一歩として、研究室で確立されていた基礎的な手法を学びながら、甲状腺に特化した新たな実験系を立ち上げていきましたが、失敗は数え切れません。大学院時代の主たるテーマとして「脱ヨード酵素の変化が甲状腺ホルモンの血中濃度に与える影響」を調べるため、ハイドロダイナミック法という遺伝子導入技術を用いて、脱ヨード酵素過剰発現マウスを開発しました(FASEB J. 36, e22141, 2022)。100を超える発現ベクターを作製し、マウスへの導入とフェノタイプ解析を繰り返したのですが、この過程で得た最大の学びは、「適切なコントロールを置き続けること」「自分のデータをよく眺めること」の重要性でした。失敗の中に前進のヒントがあり、こうした研究者としての基本を愚直に続けたことが、自分を支えてくれたと感じています。
学位取得後は、脱ヨード酵素に限らず、甲状腺生理をより包括的に理解したいという思いから、次なるプロジェクトを模索しました。新たなマウスモデルの開発に挑戦し、甲状腺機能亢進症モデルとしてTSH過剰発現マウスの開発に成功しました(iScience. 28, 111565, 2024)。また、内分泌かく乱物質に関する共同研究の機会をいただき、甲状腺機能低下症モデルを用いてホルモン作用を網羅的に評価する解析系も確立しました(iScience 26, 107135, 2023)。この頃から、「自分のオリジナルな実験系を持つ」ことの必要性を意識するようになったと思います。
これらの研究を通して、甲状腺解析における一連のワークフローを築くことができました。しかし気づけば、大学院入学当初とは環境が大きく変化しています。試薬の価格は高騰し、かつては高嶺の花だった感のあるRNA-seqは一般的となり、現在ではシングルセル解析が主流となるなど、基礎研究の高度化が進んでいます。一方で、現在は研究・教育・臨床を並行して行う大学教員として、時間的・精神的な制約も多く、すべてをカバーすることが難しくなってきました。その中で、今あらためて臨床医であることの価値を実感しています。患者を診るという経験は、医学研究を進める上で他に代えがたい視点です。ベンチとベッドサイドをつなぐ「トランスレーショナルリサーチ」を進めるうえで、実臨床を熟知していることは大きな強みになります。最近では、臨床を最前線まで把握しつつ、基礎研究者の方々と議論・協働できるよう、自らの発想力と素養をさらに磨くように努力しています。
この時代に、基礎から臨床までを見渡すPhysician Scientistであり続けることは苦難の道かもしれません。しかし、臨床が好きな方でも、研究に一度はトライしてみてください。あらかじめ答えがない問いに挑む経験や、実験をしていく際のコントロールを置く考え方は、必ず臨床に生きてきます。さらに研究が面白いと思えた方は、ぜひPhysician Scientistとして一緒にトランスレーショナルリサーチを発展させていきましょう!
経歴
2009年 京都大学医学部医学科 卒業
2009年 福井赤十字病院 初期研修医
2011年 大阪府済生会中津病院 糖尿病内分泌内科 専修医・医員
2015年 京都大学大学院医学研究科博士課程(糖尿病・内分泌・栄養内科学)入学
2019年 同上 修了
2019年 京都大学医学部附属病院 糖尿病・内分泌・栄養内科 特定病院助教
2020年 京都大学大学院医学研究科 糖尿病・内分泌・栄養内科学 助教(現職)
主な受賞歴
2017年 日本甲状腺学会 若手奨励賞
2018年 日本甲状腺学会 コスミック研究創成賞 最優秀賞
2022年 日本内科学会 第35回内科学会奨励賞
2022年 Endocrine Society Outstanding Abstract Award
2023年 日本甲状腺学会 七條賞

